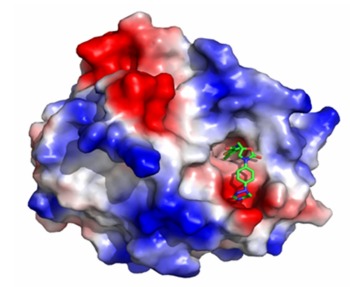
<사진자료 : Factor Xa(혈액응고 10인자)에 ‘GCC4401C’(초록색)가 결합되어 있는 모습. ‘GCC4401C’는 혈전 생성의 근본 원인인 혈액응고 10인자를 억제하여 혈전을 제거하는 ‘Factor Xa Inhibitor’ 계열의 항혈전제 신약이다.>
[아이팜뉴스=강종권기자] 녹십자가 순수 국내 기술로 개발하고 있는 항혈전제가 기존 치료제의 출혈 부작용 문제를 극복한 최초의 경구-주사 투여가 가능한 글로벌 신약으로 개발될 전망이어서 추이가 주목 된다.
녹십자는 30일 항혈전제 합성신약 ‘GCC4401C’가 미국 FDA로 부터 임상시험 승인을 받았다고 밝혔다.
녹십자가 미국에서 임상에 진입하는 ‘GCC4401C’는 혈전 생성의 주요 인자인 혈액응고 10인자를 억제하여 혈전을 제거하는 ‘Factor Xa Inhibitor’ 계열의 항혈전제로 효능이 뛰어나면서도 출혈 부작용이 적어 세계적으로 각광받고 있으며, 혈전 예방과 치료요법이 모두 가능한 장점을 가지고 있다.
기존의 치료제는 대표적 항혈전제인 저분자 헤파린과 같이 효력은 뛰어나지만 출혈 부작용이 심각하거나, 일부는 효력이 약해 다른 약물과 병용해야 하는 것이 문제점으로 지적되어 왔다.
녹십자 CTO 허은철 부사장은 “‘GCC4401C’는 비임상 시험 결과 저분자 헤파린에 비해 효력은 동등 수준이면서도, 현재 가장 안전한 치료제로 평가되는 ‘Factor Xa Inhibitor’ 계열의 기존 제품에 비해 출혈 부작용이 개선된 것으로 나타났다”고 밝혔다.
또한 “최적의 화학적 구조 설계로 용해도가 뛰어나 경구와 주사제형 모두 사용할 수 있는 최초의 약물로 기대 되며, 기존 치료제와 차별화된 경쟁력을 바탕으로 향후 해외 라이선스 아웃(License out)을 통해 글로벌 파트너와 공동개발 하여 세계시장에 출시 할 계획”이라고 밝혔다.
녹십자의 ‘GCC4401C’ 관련 특허는 미국, 유럽 등을 포함한 21개국에 출원됐으며, 내년에 미국 현지에서 임상 1상 시험을 완료한 후, 글로벌 다국가 임상시험을 실시하여 이르면 2018년 출시를 목표로 하고 있다.
현재 항혈전제의 세계 시장 규모는 20조원에 달하는 것으로 추산하고 있으며, IMS데이터에 따르면 2010년 기준 국내 시장규모는 4천억원이다.
녹십자는 지난 2009년 항혈전제 ‘GCC4401C’의 신약 후보물질을 바이오벤처인 레고켐 바이오사이언스사로 부터 도입했으며, 같은 해 지식경제부 산하 충청광역경제권 선도산업 지원단의 의약바이오 사업에도 선정되어 정부 지원을 받고 있다.